Forschungsschwerpunkte
Wir besch?ftigen uns insbesondere mit:
- Entwicklung von robusten, generalisierbaren Neuronalen Netzen (CNNs, Deep Learning)
- Daten-/Annotation-effiziente Modelle basierend auf Semi-/Self-supervised Learning
- Outlier-Detektion und Imputation von unvollst?ndige Datens?tzen
- Rekonstruktion von Bild- und Videodaten, eg. mit Hilfe von Super-Resolution
- Segmentierungsprobleme, insbesondere MRI Brain Segmentation
- Quantifizierung von Unsicherheiten von Klassifizierungsvorhersagen
- Entwicklung von interpretierbaren Features zur Verbesserung der Anwender-/Patientenkommunikation
- Evaluierung von Algorithmus Performance und Quantifizierung von Data-biases
- Translation von Forschungsergebnissen in industrielle oder medizinische Kontexte
- Quantifizierung von menschlicher Anatomie anhand von Bilddaten (MRI, X-Ray, CT) im Kontext von Erkrankungen wie Demenz, Tumoren und Traumata.
Ausgew?hlte Forschungsarbeiten
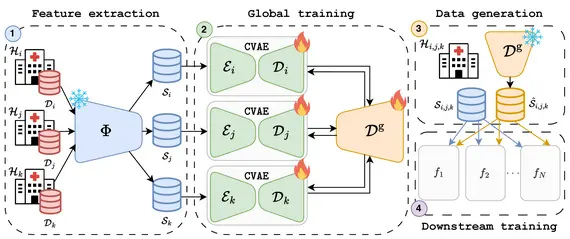
F. Di Salvo, M. Nguyen, C. Ledig, "Embedding-Based Federated Data Sharing via Differentially Private Conditional VAEs", MICCAI 2025
Deep Learning (DL) hat die medizinische Bildgebung revolutioniert. Doch seine Einführung wird durch Datenknappheit und Datenschutzbestimmungen eingeschr?nkt, wodurch der Zugang zu vielf?ltigen Datens?tzen begrenzt ist. Federated Learning (FL) erm?glicht zwar ein dezentrales Training, leidet jedoch unter hohen Kommunikationskosten und ist oft auf eine einzige nachgelagerte Aufgabe beschr?nkt, was die Flexibilit?t einschr?nkt. Wir schlagen eine Methode zum Datenaustausch über differentiell private (DP) generative Modelle vor. Mithilfe von Foundation-Modellen extrahieren wir kompakte, informative Einbettungen, wodurch Redundanzen reduziert und der Rechenaufwand gesenkt werden. Kunden trainieren gemeinsam einen Differentially Private Conditional Variational Autoencoder (DP-CVAE), um eine globale, datenschutzbewusste Datenverteilung zu modellieren, die verschiedene nachgelagerte Aufgaben unterstützt. Unser Ansatz, der für mehrere Feature-Extraktoren validiert wurde, verbessert den Datenschutz, die Skalierbarkeit und die Effizienz. Er übertrifft dabei herk?mmliche FL-Klassifikatoren, w?hrend gleichzeitig die differentielle Privatsph?re gew?hrleistet ist. Darüber hinaus erzeugt der DP-CVAE-Embedder mit h?herer Genauigkeit als der DP-CGAN-Embedder und ben?tigt dabei fünfmal weniger Parameter.
Autoren: Francesco Di Salvo*, My Nguyen*, Christian Ledig
* gemeinsame Urheberschaft
[Preprint], [Bibtex](261.0 B)
F. Di Salvo, S. Doerrich, I. Rieger, C. Ledig, "An Embedding is Worth a Thousand Noisy Labels," TMLR 2025
Die Leistung tiefer neuronaler Netze skaliert mit der Gr??e des Datensatzes und der Qualit?t der Labels. Daher ist eine effiziente Reduzierung von Datenannotationen geringer Qualit?t für den Aufbau robuster und kosteneffizienter Systeme von entscheidender Bedeutung. Aktuelle Ans?tze zur Reduktion von Label-Rauschen sind aufgrund ihrer hohen rechnerischen Komplexit?t und spezifischen Anwendungsanforderungen stark begrenzt. In dieser Arbeit pr?sentieren wir WANN, einen gewichteten adaptiven Nearest-Neighbor-Ansatz, der selbstüberwachte Merkmalsdarstellungen verwendet, die aus Basis-Modellen abgeleitet werden. Zur Steuerung des gewichteten Abstimmungsschemas führen wir einen Zuverl?ssigkeitswert ein. Dieser misst die Wahrscheinlichkeit, dass ein Datenlabel korrekt ist. WANN übertrifft Referenzmethoden – einschlie?lich einer linearen Schicht, die mit robusten Verlustfunktionen trainiert wurde – bei verschiedenen Datens?tzen unterschiedlicher Gr??e sowie unter verschiedenen Arten und Schweregraden von Rauschen. WANN zeigt auch eine überlegene Generalisierung bei unausgewogenen Daten im Vergleich zu adaptiven neuronalen Netzen (ANN) und festen k-NNs. Darüber hinaus verbessert das vorgeschlagene Gewichtungsschema die überwachte Dimensionsreduktion bei verrauschten Labels. Dies führt zu einer deutlichen Steigerung der Klassifizierungsleistung bei 10-mal und 100-mal kleineren Bild-Embeddings, wodurch sich Latenz und Speicheranforderungen minimieren lassen. Unser Ansatz, der Effizienz und Erkl?rbarkeit in den Vordergrund stellt, erweist sich somit als einfache und robuste L?sung zur ?berwindung der inh?renten Einschr?nkungen des Trainings tiefer neuronaler Netze.
Autoren: Francesco Di Salvo, Sebastian Doerrich, Ines Rieger, Christian Ledig
[Preprint], [Publication], [Code], [Bibtex](309.0 B)
S. Doerrich, F. Di Salvo, J. Brockmann, C. Ledig, “Rethinking model prototyping through the MedMNIST+ dataset collection”, Scientific Reports, 15, 7669, 2025
Die Integration von auf Deep Learning basierenden Systemen in die klinische Praxis wird h?ufig durch Herausforderungen behindert, die in begrenzten und heterogenen medizinischen Datens?tzen begründet sind. Darüber hinaus wird in diesem Bereich zunehmend marginalen Leistungssteigerungen bei einigen wenigen, eng gefassten Benchmarks Vorrang vor der klinischen Anwendbarkeit einger?umt, wodurch sinnvolle algorithmische Fortschritte verlangsamt werden. Dieser Trend führt h?ufig zu einer überm??igen Feinabstimmung bestehender Methoden an ausgew?hlten Datens?tzen, anstatt klinisch relevante Innovationen zu f?rdern. Als Reaktion darauf wird in dieser Arbeit ein umfassender Benchmark für die MedMNIST+-Datensatzsammlung eingeführt, der die Bewertungslandschaft über mehrere Bildgebungsmodalit?ten, anatomische Regionen, Klassifizierungsaufgaben und Stichprobengr??en hinweg diversifizieren soll. Wir bewerten systematisch h?ufig verwendete Convolutional Neural Networks (CNNs) und Vision Transformer (ViT)-Architekturen in verschiedenen medizinischen Datens?tzen, Trainingsmethoden und Eingabeaufl?sungen, um bestehende Annahmen über die Effektivit?t und Entwicklung von Modellen zu validieren und zu verfeinern. Unsere Ergebnisse deuten darauf hin, dass rechnerisch effiziente Trainingsverfahren und moderne Foundation-modelle praktikable Alternativen zum kostspieligen End-to-End-Training bieten. Darüber hinaus stellen wir fest, dass h?here Bildaufl?sungen die Leistung ab einem bestimmten Schwellenwert nicht durchg?ngig verbessern. Dies unterstreicht die potenziellen Vorteile der Verwendung niedrigerer Aufl?sungen, insbesondere in der Prototyping-Phase, um den Rechenaufwand zu verringern, ohne die Genauigkeit zu beeintr?chtigen. Insbesondere best?tigt unsere Analyse die Wettbewerbsf?higkeit von CNNs im Vergleich zu ViTs und unterstreicht, wie wichtig es ist, die intrinsischen F?higkeiten der verschiedenen Architekturen zu verstehen. Schlie?lich wollen wir durch die Schaffung eines standardisierten Bewertungsrahmens die Transparenz, Reproduzierbarkeit und Vergleichbarkeit innerhalb der MedMNIST+-Datensatzsammlung sowie die zukünftige Forschung verbessern.
Autoren: Sebastian Doerrich, Francesco Di Salvo, Julius Brockmann, Christian Ledig
[Preprint], [Publication], [Code], [Benchmark], [BibTeX](612.0 B)
F. Di Salvo, D. Tafler, S. Doerrich, C. Ledig, "Privacy-preserving datasets by capturing feature distributions with Conditional VAEs," BMVC 2024
Für die Weiterentwicklung von Deep-Learning-Anwendungen sind gro?e und gut annotierte Datens?tze unerl?sslich. Diese sind jedoch oft kostspielig oder für eine einzelne Einrichtung unm?glich zu beschaffen. In vielen Bereichen, darunter auch im medizinischen Bereich, haben sich Ans?tze durchgesetzt, die auf Datenaustausch basieren, um diese Herausforderungen zu bew?ltigen. Datenaustausch ist zwar wirksam, um die Gr??e und Vielfalt von Datens?tzen zu erh?hen, er wirft jedoch auch erhebliche Datenschutzbedenken auf. H?ufig verwendete Anonymisierungsmethoden, die auf dem k-Anonymit?tsparadigma basieren, k?nnen die Datenvielfalt oft nicht bewahren, wodurch die Robustheit des Modells beeintr?chtigt wird. In dieser Arbeit wird ein neuartiger Ansatz vorgestellt, der Conditional Variational Autoencoders (CVAEs) verwendet. Diese wurden auf Merkmalsvektoren trainiert, die aus gro?en, vorab trainierten Vision-Foundation-Modellen extrahiert wurden. Foundation-Modelle erkennen und repr?sentieren effektiv komplexe Muster über verschiedene Dom?nen hinweg. Dadurch kann der CVAE den Einbettungsraum einer bestimmten Datenverteilung originalgetreu erfassen, um eine vielf?ltige, datenschutzkonforme und potenziell unbegrenzte Menge synthetischer Merkmalsvektoren zu generieren (zu samplen). Unsere Methode übertrifft traditionelle Ans?tze sowohl im medizinischen als auch im natürlichen Bildbereich deutlich. Sie weist eine gr??ere Datensatzvielfalt und eine h?here Robustheit gegenüber St?rungen auf, w?hrend die Privatsph?re der Stichproben gewahrt bleibt. Diese Ergebnisse unterstreichen das Potenzial generativer Modelle, Deep-Learning-Anwendungen in datenarmen und datenschutzsensiblen Umgebungen erheblich zu verbessern.
Autoren: Francesco Di Salvo, David Tafler, Sebastian Doerrich, Christian Ledig
[Preprint], [Publication], [Code], [Bibtex](425.0 B)
F. Di Salvo, S. Doerrich, C. Ledig, "MedMNIST-C: Comprehensive benchmark and improved classifier robustness by simulating realistic image corruptions," ADSMI @ MICCAI 2025
Die Integration von Systemen auf Basis neuronaler Netze in die klinische Praxis ist aufgrund von Herausforderungen im Zusammenhang mit Dom?nengeneralisierung und Robustheit eingeschr?nkt. Die Computer-Vision-Community hat Benchmarks wie ImageNet-C als grundlegende Voraussetzung für die Messung der Fortschritte bei der Bew?ltigung dieser Herausforderungen etabliert. In der medizinischen Bildgebungsgemeinschaft fehlen ?hnliche Datens?tze weitgehend, da es an einem umfassenden Benchmark mangelt, der alle Bildgebungsmodalit?ten und -anwendungen abdeckt. Um diese Lücke zu schlie?en, haben wir den Benchmark-Datensatz MedMNIST-C erstellt und als Open Source ver?ffentlicht. Er basiert auf der MedMNIST+-Sammlung und umfasst 12 Datens?tze und 9 Bildgebungsmodalit?ten. Mithilfe von simulierten, aufgaben- und modalit?tsspezifischen Bildverf?lschungen unterschiedlicher Schwere bewerten wir die Robustheit etablierter Algorithmen gegenüber realen Artefakten und Verteilungsverschiebungen umfassend. Darüber hinaus liefern wir quantitative Belege dafür, dass unsere leicht zu verwendenden künstlichen Verf?lschungen eine leistungsf?hige und effiziente Datenvergr??erung erm?glichen und somit die Robustheit des Modells verbessern. Im Gegensatz zu traditionellen, generischen Vergr??erungsstrategien nutzt unser Ansatz Dom?nenwissen und ist im Vergleich zu weit verbreiteten Methoden deutlich robuster. Mit der Einführung von MedMNIST-C und der Ver?ffentlichung der entsprechenden Bibliothek, die gezielte Datenvergr??erungen erm?glicht, tragen wir zur Entwicklung immer robusterer, auf die Herausforderungen der medizinischen Bildgebung zugeschnittener Methoden bei.
Autoren: Francesco Di Salvo, Sebastian Doerrich, Christian Ledig
[preprint], [code],[dataset], [bibtex](291.0 B)
S. Doerrich, F. Di Salvo, C. Ledig, "Self-supervised Vision Transformer are Scalable Generative Models for Domain Generalization", MICCAI, 2024
Trotz bemerkenswerter Fortschritte wurde die Integration von Deep Learning (DL)-Techniken in wirkungsvolle klinische Anwendungen, insbesondere im Bereich der digitalen Histopathologie, durch die Herausforderungen behindert, die mit dem Erreichen einer robusten Generalisierung über verschiedene Bildgebungsdom?nen und -merkmale verbunden sind. Traditionelle Strategien in diesem Bereich wie Datenerweiterung und Fleckenfarbnormalisierung haben sich als unzureichend erwiesen, um diese Einschr?nkung zu beheben, was die Erforschung alternativer Methoden erforderlich machte. Zu diesem Zweck schlagen wir eine neuartige generative Methode zur Generalisierung von Histopathologiebildern vor. Unsere Methode verwendet einen generativen, selbstüberwachten Vision Transformer, um dynamisch Merkmale von Bildfeldern zu extrahieren und sie nahtlos in die Originalbilder einzufügen, wodurch neue, synthetische Bilder mit verschiedenen Attributen entstehen. Indem wir den Datensatz mit solchen synthetischen Bildern anreichern, wollen wir seine Ganzheitlichkeit erh?hen und eine verbesserte Generalisierung von DL-Modellen auf unbekannte Bereiche erm?glichen. Ausführliche Experimente mit zwei verschiedenen Histopathologiedatens?tzen zeigen die Effektivit?t des von uns vorgeschlagenen Ansatzes, der den Stand der Technik deutlich übertrifft, und zwar beim Camelyon17-Wilds-Datensatz (+2%) und bei einem zweiten Epithelium-Stroma-Datensatz (+26%). Darüber hinaus heben wir die F?higkeit unserer Methode hervor, mit zunehmend verfügbaren unbeschrifteten Datenproben und komplexeren, h?her parametrischen Architekturen zu skalieren.
Autoren: Sebastian Doerrich, Francesco Di Salvo, Christian Ledig
[Preprint], [Publication], [Code], [BibTeX](612.0 B)
S. Doerrich, T. Archut, F. Di Salvo, C. Ledig, "Integrating kNN with Foundation Models for Adaptable and Privacy-Aware Image Classification", IEEE ISBI, 2024
Herk?mmliche Deep-Learning-Modelle kodieren Wissen implizit, was ihre Transparenz und ihre F?higkeit zur Anpassung an Daten?nderungen einschr?nkt. Diese Anpassungsf?higkeit ist jedoch entscheidend für den Schutz der Daten der Nutzer. Wir beheben diese Einschr?nkung, indem wir die Einbettungen der zugrunde liegenden Trainingsdaten unabh?ngig von den Modellgewichten speichern und so dynamische Daten?nderungen ohne erneutes Training erm?glichen. Unser Ansatz integriert insbesondere den k-Nearest-Neighbor-Klassifikator (k-NN) mit einem bildbasierten Foundation-modell, das selbstüberwacht auf natürlichen Bildern trainiert wurde, was die Interpretierbarkeit und Anpassungsf?higkeit verbessert. Wir stellen Open-Source-Implementierungen einer bisher unver?ffentlichten Basismethode sowie unsere leistungssteigernden Beitr?ge zur Verfügung. Quantitative Experimente best?tigen die verbesserte Klassifikation in etablierten Benchmark-Datens?tzen und die Anwendbarkeit der Methode auf verschiedene medizinische Bildklassifikationsaufgaben. Darüber hinaus bewerten wir die Robustheit der Methode in Szenarien mit kontinuierlichem Lernen und Datenentfernung. Der Ansatz ist sehr vielversprechend, um die Lücke zwischen der Leistung von Foundation-modellen und den Herausforderungen des Datenschutzes zu schlie?en.
Autoren: Sebastian Doerrich, Tobias Archut, Francesco Di Salvo, Christian Ledig
[Preprint], [Publication], [Code], [BibTeX](612.0 B)